Колоректальный рак
Злокачественное новообразование толстого кишечника — злокачественная опухоль толстой кишки и её придатка — червеобразного отростка.
| Рак толстого кишечника и прямой кишки | |
|---|---|
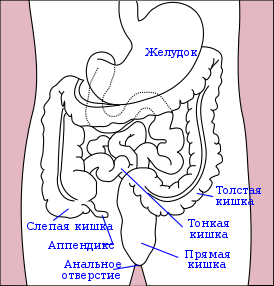 Желудок, кишечник и прямая кишка | |
| МКБ-11 | 2B91 |
| МКБ-10 | C18-C20 |
| МКБ-9 | 153.0-154.1 |
| МКБ-О | M8140/3 (95 % случаев) |
| OMIM | 114500 |
| DiseasesDB | 2975 |
| MedlinePlus | 000262 |
| eMedicine | med/413 med/1994 ped/3037 |
Вследствие неточного перевода английского термина (англ. colorectal cancer) часто обобщённую группу таких опухолей называют упрощённо колоректальным[1] раком, хотя в русском языке это более узкий термин (не включающий в себя, в частности, лимфому толстого кишечника); английский же термин охватывает также и рак прямой кишки.
Эпидемиология править
Каждый год, по данным Груздевой Е.С., в мире выявляется более 600 тысяч новых случаев рака толстой кишки. В России заболеваемость составляет около 50 тысяч новых случаев в год. Далеко не все случаи колоректального рака выявляются даже на поздней стадии, показатель составляет не более 70 %.
Этиология править
Рак толстой кишки — полиэтиологическое заболевание, то есть может иметь под собой множество причин. К ним относятся: генетические факторы, факторы внешней среды (включая питание, канцерогены), воспалительный процесс в кишечнике.
Хотя генетика колоректального рака остаётся до конца не раскрытой, последние исследования показывают её большое значение в развитии болезни. Так, наследственная мутация в гене APC является причиной семейного аденоматозного полипоза, при котором у пациента имеется почти 100%-я вероятность развития рака толстой кишки к возрасту 40 лет[2].
В возникновении колоректального рака прослеживается два пути: из обычных аденом, начинающийся с мутации гена APC (модель Fearon-Vogelstein) и по «зубчатому пути», который отличается уникальным генетическим профилем и морфологическими характеристиками уже на начальных этапах развития образований. Такие образования занимают от 7-9 %. Риск развития рака из них составляет 7,5-15 %. Предшественниками эпителиальных образований являются очаги аберрантных крипт. Около 20 % колоректального рака продемонстрировали распространённые дефекты в метилировании ДНК (так называемый CIMP-положительный профиль), мутации в онкогенах BRAF (KRAS), микросателлитную нестабильность, и многие из них могут возникнуть в рамках зубчатых образований и определяют их морфологическое строение. Зубчатый полипозный синдром так же имеет специфические генетические изменения, связанные с биаллельной мутацией гена MUTYH. Риск развития колоректального рака при этом синдроме очень высок и может составлять более 50 %, возможно наличие синхронных или метахронных раковых опухолей. Они, как правило, сопровождаются MSI-H и представлены зубчатой морфологией. Понимание эпигенетического пути и молекулярных особенностей зубчатых поражений даёт представление об их клинической значимости и обеспечивает доказательства, необходимые для лечения и наблюдения пациентов с этим заболеванием.
Синдром Линча (наследственный рак толстой кишки без полипоза) также связан с высоким риском возникновения рака толстой кишки в возрасте до 50 лет. В отличие от семейного аденоматозного полипоза, при синдроме Линча чаще страдает проксимальный отдел толстой кишки. Пациенты с данным синдромом также подвержены высокому риску развития рака яичников и тела матки в молодом возрасте. Синдром обусловлен ошибками репликации в генах hMLH1, hMSH2, hMSH6, hPMS1, hPMS2 и, возможно, других, ещё не известных[3][4][5].
Факторы риска править
- Диетические — употребление пищи, бедной клетчаткой и богатой твёрдыми животными жирами.
- Употребление алкоголя[6].
- Ожирение.
- Курение[7].
- Воспалительные заболевания кишечника.
По результатам исследования, опубликованным в Журнале Клинической Онкологии (Journal of Clinical Oncology), курильщики с раком толстого кишечника имеют в два раза более высокий риск смерти по сравнению с некурящими людьми[8].
Также была проведена работа, опубликованная в журнале Gut (The BMJ journals), результаты которой свидетельствуют, что длительное применение антибиотиков в молодом и среднем возрасте увеличивает риск появления колоректальных аденом, склонных к малигнизации[9]. Учёные исследовали связь между длительной антибиотикотерапией (более 2 месяцев) в возрасте 20-39 лет и 40-59 лет с развитием аденоматозных полипов. Все участники прошли колоноскопию, по результатам которой было выявлено, что у 1195 из 16642 участников обнаружены колоректальные аденомы. Проведя анализ доступных данных, исследователи заключили, что применение антибиотиков более 2 месяцев у лиц в возрасте 20-39 лет приводит к риску возрастания полипов на 36 %, а в возрасте 20-59 лет — на 69 %. Высокий риск перехода аденомы в злокачественную опухоль был подтверждён многочисленными исследованиями. Риск развития рака прямой и ободочной кишки у лиц с аденоматозными полипами в 3-5 раз выше, чем у обычной популяции.
Диагностика править
- Колоноскопия с биопсией
- Ирригоскопия
- СКТ органов малого таза, брюшной полости
- УЗИ ОБП, ОМТ
- Анализ крови на метилирование гена SEPT9
Прогноз править
По причине поздней диагностики летальность от этого заболевания довольно высока и достигает 40 % в течение года с момента выявления болезни.
Наиболее частым органом, в который метастазирует колоректальный рак, является печень. Это обусловлено особенностями венозного оттока от кишечника, который осуществляется через систему воротной вены печени. По данным некоторых авторов, наличие метастазов в печени при колоректальном раке достигает 50 % (Curtiss, 1995).
Другим частым местом рецидива колоректального рака является брюшина. Перитонеальный канцероматоз выявляется примерно у 10 % пациентов с только что установленным диагнозом. В случае рецидива брюшина поражается примерно в 60 % изолированно либо вместе с печенью.
По данным Viganò, пятилетняя выживаемость у пациентов с метастазами колоректального рака в печени без специфического лечения не превышает 2 %, а медиана выживаемости колеблется в пределах 6,6—10 мес[10].
В настоящее время смертность после резекций печени по поводу метастазов колоректального рака составляет менее 6 %, а в крупных специализированных клиниках - менее 3 %[11].
Лечение править
Большинство пациентов с установленным раком толстой кишки являются кандидатами на операцию. Суть операции заключается в удалении части толстой кишки, несущей опухоль, и лимфоузлов, в которых могут быть обнаружены метастазы.
Послеоперационное гистологическое исследование обязательно во всех случаях. Во время него оценивается удалённый орган: сохранность мезоректальной или мезоколической фасций, уровень инвазии опухоли, количество лимфатических узлов в препарате и сколько из них поражены метастазами, расстояние от опухоли до края резекции.
Химиотерапия (FOLFIRI и др.).
Химиотерапия в сочетании с кетогенной диетой в одном исследовании на малом числе пациентов показала чуть более хорошие результаты[12][значимость факта?]
Моноклональные антитела: ипилимумаб, ниволумаб, рамуцирумаб.
Другие препараты: фруквинтиниб.
Примечания править
- ↑ от лат. colon «ободочная кишка» + rectum «прямая кишка»
- ↑ Tomislav Dragovich, MD, PhD. Colon Cancer (англ.). Medscape. Дата обращения: 8 октября 2015. Архивировано 23 сентября 2015 года.
- ↑ Lengauer C., Kinzler K. W., Vogelstein B. Genetic instabilities in human cancers //Nature. — 1998. — Т. 396. — №. 6712. — С. 643—649.
- ↑ Lynch H. T. et al. Etiology, natural history, management and molecular genetics of hereditary nonpolyposis colorectal cancer (Lynch syndromes): genetic counseling implications //Cancer Epidemiology Biomarkers & Prevention. — 1997. — Т. 6. — №. 12. — С. 987—991.
- ↑ Angioli R. et al. Hereditary and sporadic ovarian cancer: genetic testing and clinical implications (review) //International journal of oncology. — 1998. — Т. 12. — №. 5. — С. 1029—1063.
- ↑ Колоректальный рак. www.euro.who.int (5 февраля 2018). Дата обращения: 5 февраля 2018. Архивировано 30 января 2018 года.
- ↑ Модифицируемые факторы риска развития рака. // Факторы риска развития рака. Пер. с англ. Н. Д. Фирсова(2017).
- ↑ Baiyu Yang, Eric J. Jacobs, Susan M. Gapstur, Victoria Stevens, Peter T. Campbell. Active Smoking and Mortality Among Colorectal Cancer Survivors: The Cancer Prevention Study II Nutrition Cohort // Journal of Clinical Oncology. — 2015-01-01. — Т. 33, вып. 8. — С. 885–893. — ISSN 0732-183X. — doi:10.1200/JCO.2014.58.3831. Архивировано 17 октября 2020 года.
- ↑ Long-term use of antibiotics and risk of colorectal adenoma Архивная копия от 14 апреля 2017 на Wayback Machine Длительное применение антибиотиков и риск колоректальной аденомы
- ↑ Viganò L., Ferrero A., Lo Tesoriere R., Capussotti L. Liver surgery for colorectal metastases: results after 10 years of follow-up. Long-term survivors, late recurrences, and prognostic role of morbidity // Ann Surg Oncol, 2008, 15 (9). — P. 2458—2464. Epub 2008 May 8.
- ↑ Wang X., Hershman D. L., Abrams J. A., Feingold D., Grann V. R., Jacobson J. S., Neugut A. I. Predictors of survival after hepatic resection among patients with colorectal liver metastasis // British Journal of Cancer, 2007, 97 (12). — P. 1606—1612. Epub 2007 Dec 11.
- ↑ Kenji Furukawa, Kyosuke Shigematus, Yoshie Iwase, Wakako Mikami, Hiroko Hoshi. Clinical effects of one year of chemotherapy with a modified medium-chain triglyceride ketogenic diet on the recurrence of stage IV colon cancer. // Journal of Clinical Oncology. — 2018-05-20. — Т. 36, вып. 15_suppl. — С. e15709–e15709. — ISSN 0732-183X. — doi:10.1200/JCO.2018.36.15_suppl.e15709. Архивировано 1 ноября 2020 года.