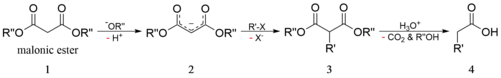Малоновый эфир
Мало́новый эфи́р (диэтиловый эфир малоновой кислоты, диэтилмалонат) — органическое соединение, сложный эфир малоновой кислоты и этилового спирта с химической формулой C2H5OOCCH2COOC2H5. Бесцветная жидкость с фруктовым запахом. Используется в органическом синтезе, в производстве лекарственных средств и в пищевой промышленности как ароматизатор.
| Малоновый эфир | |||
|---|---|---|---|
| |||
| Общие | |||
| Хим. формула | C7H12O4 | ||
| Физические свойства | |||
| Молярная масса | 160,18 г/моль | ||
| Плотность | 1,0553 г/см³ | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -49,8 °C | ||
| • кипения | 198,9 °C | ||
| Классификация | |||
| Рег. номер CAS | 105-53-3 | ||
| PubChem | 7761 | ||
| Рег. номер EINECS | 203-305-9 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 167785 | ||
| ChemSpider | 13863636 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Механизм править
Углерод в альфа положении карбонильных групп может быть депротонирован сильным основанием. Образовавшийся карбанион может подвергнуться нуклеофильному замещению алкилгалогенида с образованием алкилированного соединения. При нагревании диэфир подвергается термическому декарбоксилированию с образованием уксусной кислоты, замещенной соответствующей группой R. Таким образом, малоновый эфир можно считать эквивалентным -CH 2 COOH .
Выбранные эфиры обычно такие же, как и используемое основание, т.е. этиловые эфиры с этоксидом натрия . Это делается для предотвращения скремблирования путем переэтерификации .
Синтезы править
Диалкилирование править
Сложный эфир можно диалкилировать, если депротонирование и алкилирование повторяют перед добавлением водной кислоты.
Синтез циклоалкилкарбоновой кислоты править
Синтез внутримолекулярного малонового эфира происходит при взаимодействии с дигалогенидом . Эта реакция также называется алициклическим синтезом Перкина в честь исследователя Уильяма Генри Перкина-младшего
Другие синтезы править
также с помощью малонового эфира можно получать
- дикарбоновые кислоты (янтарную, адипиновую и др.)
- непредельные карбоновые кислоты через галогеналкены (кроме альфа- и бета- непредельных)
- альфа- и бета- непредельные карбоновые кислоты через альдегиды и кетоны по реакции Кнёвенагеля (акриловую и др.)
- бета-аминокислоты по реакции Родионова
Свойства править
Бесцветная маслянистая жидкость с запахом фруктов. Имеет молярную массу 160,18 г/моль. Плавится при температуре -49,8 °C, кипит при 198,9 °C (760 мм рт. ст.), 92 °C (18 мм. рт. ст.). Имеет относительную плотность = 1,0553, показатель преломления = 1,41428. Смешивается в любых отношениях с этиловым спиртом, эфиром, этилацетатом, плохо растворим в воде (2,124 г/100 г)[1].
Атомы водорода в группе CH2 имеют высокую подвижность и благодаря им соединение легко образует металлические производные[1].
Применение править
В производстве лекарственных средств малоновый эфир используется для синтеза барбитуратов, а также седативных и антиконвульсивных средств.
Помимо этого, находит применение в органическом синтезе[1] .
В пищевой промышленности применяется как ароматизатор[1].
Примечания править
- ↑ 1 2 3 4 Попова, 1990.
Литература править
- Попова Р. Я. Малоновый эфир // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1990. — Т. 2: Даффа — Меди. — С. 641—642. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.