Супрамолекулярная сборка
Супрамолекулярная сборка (англ. supramolecular assembly, надмолекулярная сборка) представляет собой комплекс молекул, удерживаемых вместе нековалентными связями. В то время как супрамолекулярная сборка может состоять просто из двух молекул (например, двойной спирали ДНК или соединения включения) или из определённого числа стехиометрически взаимодействующих молекул внутри четвертичного комплекса, она чаще используется для обозначения более крупных комплексов, состоящих из неопределенного числа молекул. молекул, образующих сферические, палочковидные или пластинчатые формы. Коллоиды, жидкие кристаллы, биомолекулярные конденсаты, мицеллы, липосомы и биологические мембраны являются примерами надмолекулярных ансамблей[3]. Размеры супрамолекулярных ансамблей могут варьироваться от нанометров до микрометров. Таким образом, они позволяют получить доступ к наноразмерным объектам, используя подход «снизу вверх», за гораздо меньшее количество шагов, чем одна молекула аналогичных размеров.
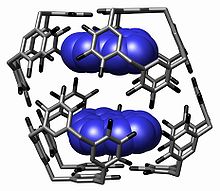

Процесс образования супрамолекулярной сборки называется молекулярной самосборкой. Некоторые пытаются определить самосборку как процесс, посредством которого отдельные молекулы образуют определённый агрегат. Таким образом, самоорганизация — это процесс, посредством которого эти агрегаты создают структуры более высокого порядка. Это может оказаться полезным, когда речь идет о жидких кристаллах и блок-сополимерах.
Шаблонные реакции править
Как изучается в координационной химии, ионы металлов (обычно ионы переходных металлов) существуют в растворе, связанные с лигандами. Во многих случаях координационная сфера определяет геометрию, способствующую реакциям либо между лигандами, либо с участием лигандов и других внешних реагентов.
Хорошо известное шаблонирование ионами металлов было описано Чарльзом Педерсеном в его синтезе различных краун-эфиров с использованием катионов металлов в качестве шаблона. Например, 18-краун-6 сильно координирует ион калия, поэтому его можно получить путем синтеза эфира Вильямсона с использованием иона калия в качестве металла-шаблона.
Ионы металлов часто используются для сборки больших супрамолекулярных структур. Металлоорганические каркасы (MOF) являются одним из примеров[4]. MOF представляют собой бесконечные структуры, в которых металлы служат узлами для соединения органических лигандов. SCC представляют собой дискретные системы, в которых выбранные металлы и лиганды подвергаются самосборке с образованием конечных надмолекулярных комплексов[5], обычно размер и структура образующегося комплекса могут определяться угловатостью выбранных связей металл-лиганд.
Супрамолекулярная сборка с помощью водородной связи править
Супрамолекулярная сборка с помощью водородных связей — это процесс сборки небольших органических молекул с образованием больших супрамолекулярных структур за счет взаимодействий нековалентных водородных связей. Направленность, обратимость и прочная природа водородной связи делают её привлекательным и полезным подходом к супрамолекулярной сборке. Функциональные группы карбоновых кислот, мочевины, аминов и амидов обычно используются для сборки структур более высокого порядка с помощью водородных связей.
Водородные связи играют существенную роль в сборке вторичных и третичных структур больших биомолекул. Двойная спираль ДНК образуется за счет водородных связей между азотистыми основаниями: аденин и тимин образуют две водородные связи, а гуанин и цитозин образуют три водородные связи (рисунок «Водородные связи в (а) образовании дуплекса ДНК»). Другим ярким примером сборки с помощью водородных связей в природе является образование вторичных структур белка. И α-спираль, и β-лист образуются за счет водородных связей между амидным водородом и амидным карбонильным кислородом (рисунок «Водородные связи в (b) структуре β-листа белка»).
В супрамолекулярной химии водородные связи широко применяются в инженерии кристаллов, молекулярном распознавании и катализе[6][7]. Водородные связи являются одними из наиболее часто используемых синтонов в подходе «снизу вверх» к инженерным молекулярным взаимодействиям в кристаллах. Репрезентативные модели водородных связей для супрамолекулярной сборки показаны на рисунке «Репрезентативные модели водородных связей в супрамолекулярной сборке»[8]. Смесь 1:1 циануровой кислоты и меламина образует кристалл с очень плотной сеткой водородных связей. Эти надмолекулярные агрегаты использовались в качестве шаблонов для создания других кристаллических структур[9].
Применение править
Супрамолекулярные сборки не имеют конкретных применений, но являются предметом многих интригующих реакций. Показано, что надмолекулярная сборка пептидных амфифилов в виде нановолокон способствует росту нейронов[10]. Преимущество этого супрамолекулярного подхода заключается в том, что нановолокна снова распадаются на отдельные пептидные молекулы, которые могут быть расщеплены организмом. Путем самосборки дендритных дипептидов можно получить полые цилиндры. Цилиндрические сборки обладают внутренним спиральным порядком и самоорганизуются в столбчатые жидкокристаллические решетки. При введении в везикулярные мембраны пористые цилиндрические сборки опосредуют перенос протонов через мембрану [11]. Самосборка дендронов порождает массивы нанопроволок[12]. Электронодонорно-акцепторные комплексы составляют ядро цилиндрических супрамолекулярных ансамблей, которые в дальнейшем самоорганизуются в двумерные столбчатые жидкокристаллические решетки. Каждая цилиндрическая надмолекулярная сборка функционирует как отдельная проволока. Получены высокие подвижности носителей заряда для дырок и электронов.
См. также править
Примечания править
- ↑ Dalgarno, S. J. (2005). "Fluorescent Guest Molecules Report Ordered Inner Phase of Host Capsules in Solution". Science. 309 (5743): 2037—9. Bibcode:2005Sci...309.2037D. doi:10.1126/science.1116579. PMID 16179474.
- ↑ Hasenknopf, Bernold (1996). "Self-Assembly of a Circular Double Helicate". Angewandte Chemie International Edition in English. 35 (16): 1838. doi:10.1002/anie.199618381.
- ↑ Ariga, Katsuhiko (2008). "Challenges and breakthroughs in recent research on self-assembly". Science and Technology of Advanced Materials. 9 (1): 014109. Bibcode:2008STAdM...9a4109A. doi:10.1088/1468-6996/9/1/014109. PMID 27877935.
- ↑ Cook, T. R.; Zheng, Y.; Stang, P. J. (2013). "Metal-organic frameworks and self-assembled supramolecular coordination complexes: Comparing and contrasting the design, synthesis, and functionality of metal-organic materials". Chem. Rev. 113 (1): 734—77. doi:10.1021/cr3002824. PMID 23121121.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Paul, R. L.; Bell, Z. R.; Jeffery, J. C.; McCleverty, J. A.; Ward, M. D. (2002). "Anion-templated self-assembly of tetrahedral cage complexes of cobalt(II) with bridging ligands containing two bidentate pyrazolyl-pyridine binding sites". Proc. Natl. Acad. Sci. 99 (8): 4883—8. Bibcode:2002PNAS...99.4883P. doi:10.1073/pnas.052575199. PMID 11929962.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Lehn, J. M. (1985). "Supramolecular chemistry: Receptors, catalysts, and carriers". Science. 227 (4689): 849—56. Bibcode:1985Sci...227..849L. doi:10.1126/science.227.4689.849. PMID 17821215.
- ↑ Meeuwissen, J.; Reek, J. N. H. (2010). "Supramolecular catalysis beyond enzyme mimics". Nat. Chem. 2 (8): 615—21. Bibcode:2010NatCh...2..615M. doi:10.1038/nchem.744. PMID 20651721.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Desiraju, G. R. (2013). "Crystal engineering: From molecule to crystal". J. Am. Chem. Soc. 135 (27): 9952—67. doi:10.1021/ja403264c. PMID 23750552.
- ↑ Seto, C. T.; Whitesides, G. M. (1993). "Molecular self-assembly through hydrogen bonding: Supramolecular aggregates based on the cyanuric acid-melamine lattice". J. Am. Chem. Soc. 115 (3): 905—916. doi:10.1021/ja00056a014.
{{cite journal}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка) - ↑ Gabriel A. Silva, Catherine Czeisler, Krista L. Niece, Elia Beniash, Daniel A. Harrington, John A. Kessler, Samuel L. Stupp. Selective Differentiation of Neural Progenitor Cells by High-Epitope Density Nanofibers (англ.) // Science Magazine. — 2004. — 27 February. Архивировано 22 сентября 2022 года.
- ↑ Percec, Virgil; Dulcey, Andrés E.; Balagurusamy, Venkatachalapathy S. K.; Miura, Yoshiko; Smidrkal, Jan; Peterca, Mihai; Nummelin, Sami; Edlund, Ulrica; Hudson, Steven D.; Heiney, Paul A.; Duan, Hu; Magonov, Sergei N.; Vinogradov, Sergei A. Self-assembly of amphiphilic dendritic dipeptides into helical pores (англ.) // Nature. — 2004. — doi:10.1038/nature02770|10.1038/nature02770. — PMID 15306805.
- ↑ Percec, V.; Glodde, M.; Bera, T. K.; Miura, Y.; Shiyanovskaya, I.; Singer, K. D.; Balagurusamy, V. S. K.; Heiney, P. A.; Schnell, I.; Rapp, A.; Spiess, H.-W.; Hudson, S. D.; Duan, H. Self-organization of supramolecular helical dendrimers into complex electronic materials (англ.) // Nature. — 2002. — doi:10.1038/nature01072|10.1038/nature01072. — PMID 12352988. Архивировано 20 декабря 2016 года.
На эту статью не ссылаются другие статьи Википедии. |