Хлорид кобальта(II)
Хлори́д ко́бальта(II) (дихлори́д ко́бальта) — неорганическое соединение, кобальтовая соль соляной (хлороводородной) кислоты с формулой CoCl2. Относится к классу галогенидов кобальта.
| Хлорид кобальта(II) | |
|---|---|
 | |
 | |
| Общие | |
| Систематическое наименование |
Хлорид кобальта(II) |
| Традиционные названия | хлорид кобальта(2+); двуххлористый кобальт |
| Хим. формула | CoCl2 |
| Рац. формула | CoCl2 |
| Физические свойства | |
| Состояние | твёрдое |
| Молярная масса | 129,84 г/моль |
| Плотность |
3,356 г/см3 гексагидрат: 1,92 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 735 °C |
| • кипения | 1049 °C |
| Энтальпия | |
| • образования | −310 кДж/моль |
| Классификация | |
| Рег. номер CAS | 7646-79-9 |
| PubChem | 24288 и 3032536 |
| Рег. номер EINECS | 231-589-4 |
| SMILES | |
| InChI | |
| RTECS | GF9800000 |
| ChEBI | 35696 |
| Номер ООН | 3288 |
| ChemSpider | 22708 |
| Безопасность | |
| ЛД50 | 80 мг/кг |
| Токсичность | весьма ядовит |
| Краткие характер. опасности (H) |
H302, H317, H318, H334, H341, H350i, H360F, H410 |
| Меры предостор. (P) |
P201, P261, P273, P280, P284 |
| Сигнальное слово | опасно |
| Пиктограммы СГС |
|
| NFPA 704 | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |

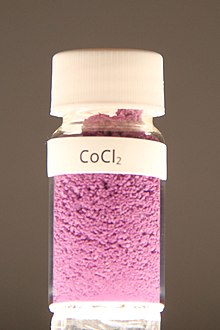

Хлорид кобальта(II) гигроскопичен. Известны кристаллогидраты CoCl2·nН2О (n = 1, 2, 4, 5, 6):
- сине-фиолетовый моногидрат (устойчив на воздухе до 110 °C, т. пл. 335 °C, с разложением);
- фиолетовый дигидрат (устойчив до 90 °C, т. пл. 206 °C, с разложением);
- темно-красный тетрагидрат;
- красный пентагидрат;
- розовый гексагидрат (т. пл. 51,2 °C, с разложением) — хлорид кобальта шестиводный: CoCl2·6H2O;
Физические свойства
правитьБезводный дихлорид кобальта при нормальных условиях представляет собой парамагнитные гигроскопичные блестящие голубые гексагональные кристаллы, при нагреве до 680°C переходит в другую полиморфную модификацию.
- Молекулярная масса безводного вещества: 129,84.
- Температура кипения: 1049 °C.
- Температура плавления: 735 °C (по другим источникам 724 °C).
- Теплота плавления 38 кДж/моль.
- Теплота испарения 14,5 кДж/моль.
- Теплоёмкость 78,49 Дж/(моль·К).
- Молярная электропроводность при бесконечном разведении при 25 °C равна 260,7 См·см²/моль.
- Плотность: 3,356 г/см3.
- Давление паров при 770 °C: 5,33 кПа.
- Хорошо растворим в воде, метиловом и этиловом спиртах, ацетоне.
- Не растворяется в пиридине и метилацетате.
Растворимость в воде:
- при 7 °C 45,0 г/100 мл;
- при 20 °C 52,9 г/100 мл.
Химические свойства
правитьРастворяется в воде, образуя катион [Co(H2O)6]2+, который придаёт раствору окраску:
Может вступать в реакции двойного обмена как по катиону, так и по аниону:
Может быть восстановлен до кобальта более активными металлами или электролизом:
Склонен к комплексообразованию. Например, с аммиаком, цианат-ионом:
Получение
править- действием хлора на нагретый до 850—900 °C порошкообразный кобальт;
- растворением металлического кобальта, его оксида CoO, гидроксида Co(OH)2 или карбоната CoCO3 в НСl с последующей дегидратацией в вакууме при 150 °C или обработкой тионилхлоридом SOCl2.
- безводный — дегидратацией кристаллогидратов CoCl2·nН2О;
Применение
править- Применяют в метеорологии для изготовления индикаторной бумаги, с помощью которой определяют атмосферную влажность.
- протравы при крашении тканей,
- микродобавки в корм скоту,
- компоненты растворов для нанесения кобальтовых покрытий на металлы
- индикатор влажности в составе силикагеля, используется свойство изменения окраски кристаллогидрата при увеличении количества захваченных молекул воды.
- для получения катализаторов
- Хлорид кобальта придает стеклянной массе синюю окраску, поэтому он применяется для производства синего и голубого декоративного стекла.
- Хлорид кобальта образует прочные связи с циан-ионом. Это навело на мысль использовать хлорид кобальта в качестве антидота при отравлении цианидами. Хотя был получен положительный эффект, сами соли кобальта обладают высокой общей токсичностью по отношению к людям. В больших дозах они являются канцерогенами.
- для низкотемпературного капсулирования порошка гамма-оксида железа(III) ферритом кобальта(II) в производстве магнитных лент[1].
Токсичность
правитьКак и некоторые другие соединения кобальта, его хлорид ядовит для человека в больших концентрациях.
См. также
править- Хлорид кобальта(III) CoCl3
Источники
править- ↑ Mallinson J. C. The Foundations of Magnetic Recording. — Elsevier, 2012. — P. 31. — ISBN 9780080506821.
- Раков Э. Г. Кобальта галогениды // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1990. — Т. 2: Даффа — Меди. — С. 416. — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
- Лурье Ю. Ю. Справочник по аналитической химии. — М.: Химия, 1989
- Фримантл М. Химия в действии. Т. 2. М.: Мир, 1991
