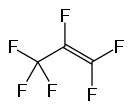
Гексафторпропилен
1,1,2,3,3,3-Гексафторпропилен — относится к фторолефинам – алкенам, в которых один или несколько атомов водорода замещены атомами фтора. Является непредельным фторорганическим соединением и служит в качестве мономера (Мономер-6) для синтеза термостойких и химически стойких полимеров и сополимеров (фторопластов и фторкаучуков).
| 1,1,2,3,3,3-Гексафторпропилен | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
1,1,2,3,3,3-Гексафторпропилен | ||
| Традиционные названия | Гексафторпропилен, Перфторпропилен, Мономер-6 (М-6) | ||
| Хим. формула | C3F6 | ||
| Рац. формула | CF2CFCF3 | ||
| Физические свойства | |||
| Состояние | бесцветный газ | ||
| Молярная масса | 150,02 г/моль | ||
| Энергия ионизации | 10,6 эВ[1] | ||
| Термические свойства | |||
| Температура | |||
| • плавления | -156,5 °C | ||
| • кипения | -29,4 °C | ||
| Критическая точка |
температура: 85 °C давление: 3,15 МПа плотность: 0,6 г/см³ |
||
| Классификация | |||
| Рег. номер CAS | 116-15-4 | ||
| PubChem | 8302 | ||
| Рег. номер EINECS | 204-127-4 | ||
| SMILES | |||
| InChI | |||
| RTECS | UD0350000 | ||
| ChemSpider | 8001 | ||
| Безопасность | |||
| NFPA 704 | |||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Свойства править
Физические свойства править
Бесцветный газ. Практически не имеет запаха, тяжелее воздуха, раздражает дыхательные пути. ПДК составляет 5 мг/м³; летальная концентрация 0,3 % по объёму. Не образует взрывоопасных смесей с воздухом.
Химические свойства править
Гексафторпропилен практически не даёт гомополимеров[2].
По радикальному механизму мономер-6 галогенируется, легко присоединяет H2S, NaHSO3, спирты, простые эфиры (атака направляется на CF2-rpyппy).
Получение править
Впервые получен А. Хэнне и Т. Валкесом в 1945 году[2].
Промышленным способом получения гексафторпропилена является пиролиз тетрафторэтилена при 700—900 °С[2].
Гексафторпропилен может быть получен путём термической обработки тетрафторэтилена, хлортетрафторэтана или октафторциклобутана и совместного пиролиза хлордифторметана и 2-хлор-1,1,1,2-тетрафторэтана, декарбоксилированием солей перфтормасляной кислоты.
Применение править
Гексафторпропилен используется в качестве технологического газа в плазменной технологии для нанесения ПТФЭ-подобных слоев на поверхности. Он выступает в качестве сомономера для промышленного получения полимеров на основе тетрафторэтилена и винилиденфторида.
Ссылки править
- Химический энциклопедический словарь / гл. ред. И. Л. Кнунянц. — М.: Сов. энциклопедия, 1983. — С. 638. — 792 с.
Примечания править
- ↑ David R. Lide, Jr. Basic laboratory and industrial chemicals (англ.): A CRC quick reference handbook — CRC Press, 1993. — ISBN 978-0-8493-4498-5
- ↑ 1 2 3 Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.