Озоновый слой
Озо́новый слой — часть стратосферы на высоте от 20 до 40 км (в тропических широтах 25—30 км, в умеренных 20—25, в полярных 15—20) с наибольшим содержанием озона (вещества, молекула которого состоит из трёх атомов кислорода, O3), образующегося в результате воздействия УФ-излучения Солнца на молекулярный кислород (O2). При распаде кислорода, атомы которого затем образуют озон, поглощается ближняя (к видимому свету) часть ультрафиолета солнечного спектра. Кроме того, диссоциация озона под воздействием ультрафиолетового излучения приводит к поглощению наиболее жёсткой его части.
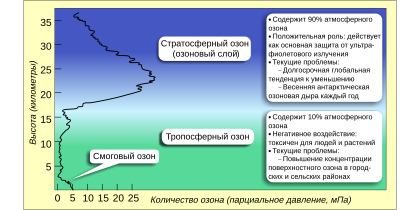

Около 90 % атмосферного озона находится в стратосфере, главным образом на высоте от 20 до 40 км над поверхностью Земли. Его концентрация в стратосфере составляет от 2 до 8 частей на миллион. Общее количество озона в атмосфере таково, что если бы можно было весь его переместить на уровень моря и сконцентрировать до атмосферного давления при температуре 0 °C, он занял бы слой высотой всего 3 мм (это соответствует 300 единицам Добсона, или 300×2,69×1016 молекул озона на квадратный сантиметр поверхности Земли). Для сравнения, вся сжатая под нормальным давлением атмосфера составляла бы слой в 8 км. Озоновый слой поглощает от 97 до 99 % солнечного излучения в области длин волн от 200 до 315 нм.
Очень опасный ультрафиолет в диапазоне UV-c (100—280 нм) практически полностью поглощается кислородом (< 200 нм с образованием монокислорода и далее озона) и озоном (200—280 нм) в самых верхних слоях атмосферы, выше 35 км. Диапазон UV-b (280—315 нм), вызывающий загар и рак кожи, поглощается озоном почти полностью, до поверхности Земли доходит лишь несколько процентов, причём в длинноволновой части этого диапазона, тогда как на длине волны 290 нм коэффициент поглощения озонового слоя составляет 3,5×108. Диапазон UV-a (315—400 нм), ближайший к видимому свету (400—700 нм), почти не поглощается (см. рис.)[1].
Благодаря нагреванию воздуха вследствие поглощения озоном солнечных лучей возникает температурная инверсия, то есть повышение температуры с высотой. Таким образом, тропосфера и стратосфера разделяются тропопаузой и смешивание воздуха между этими слоями атмосферы затруднено.
Озоновый слой образовался в атмосфере Земли 1,85—0,85 млрд лет назад, когда в ней вследствие фотосинтеза накопилось достаточно кислорода[2]. Лишь после образования озонового слоя жизнь (включая растения) смогла выйти из океанов[3]; без этого высокоразвитые формы жизни типа млекопитающих, включая человека, не возникли бы.
История открытия озонового слоя
правитьОткрывателями озонового слоя были французские физики Шарль Фабри и Анри Буиссон. В 1912 году им удалось с помощью спектроскопических измерений ультрафиолетового излучения доказать существование озона в отдалённых от Земли слоях атмосферы.
Благодаря данным ультрафиолетового спектрометра, работавшего на борту орбитального зонда Venus Express, астрономы обнаружили озоновый слой в атмосфере Венеры[4][5].
Механизм Чепмена
правитьМеханизм образования, а также расходования озона был предложен Сидни Чепменом в 1930 году и носит его имя.
Реакции образования озона:
Фотолиз молекулярного кислорода происходит в стратосфере под воздействием ультрафиолетового излучения с длиной волны 175—200 нм и до 242 нм.
Озон расходуется в реакциях фотолиза и взаимодействия с атомарным кислородом:
Пути гибели озона
правитьКроме реакций, входящих в механизм Чепмена, имеется целый ряд других реакций, приводящих к гибели озона. Их все объединяют в несколько семейств, главными из которых является азотное, кислородное (из механизма Чепмена), водородное и галогеновое. Эти реакции представляют собой каталитические циклы, поэтому их также называют соответствующими циклами.
Азотный цикл (NOx):
Водородный цикл (HOx):
Хлорный цикл (ClOx):
Доля в расходовании озона различных химических семейств на разных высотах:[6]
| Давление, гПа | азотное | кислородное | водородное | галогеновое |
|---|---|---|---|---|
| 1,31 | 0,10 | 0,26 | 0,41 | 0,21 |
| 3,78 | 0,50 | 0,14 | 0,11 | 0,25 |
| 8,93 | 0,68 | 0,11 | 0,08 | 0,13 |
| 21,9 | 0,46 | 0,12 | 0,19 | 0,20 |
| 55,8 | 0,12 | 0,03 | 0,48 | 0,14 |
Доля галогенового пути распада стратосферного озона увеличилась в результате деятельности человека, что привело к возникновению озоновых дыр. Генеральная ассамблея ООН в 1994 году провозгласила 16 сентября ежегодным Международным днём охраны озонового слоя.
Единица измерения толщины озонового слоя
правитьЕдиницей измерения толщины озонового слоя служит единица Добсона (DU).
Примечания
править- ↑ Matsumi Y., Kawasaki M. Photolysis of Atmospheric Ozone in the Ultraviolet Region (англ.) // Chem. Rev.[англ.] : journal. — 2003. — Vol. 103, no. 12. — P. 4767—4781. — doi:10.1021/cr0205255. — PMID 14664632.
- ↑ Gehrels N., Claude M. Laird, Charles H. Jackman, John K.M. Cannizo, Barbara J. Mattson, Wan Chen (2003) Ozone Depletion from Nearby Supernovae. The Astrophysical Journal, 585 : 1169—1176.
- ↑ И. К. Ларин. Химия озонового слоя и жизнь на Земле // Химия и жизнь — XXI век. — 2000. — № 7. — С. 10—15.
- ↑ Discovery of cloud top ozone on Venus. Дата обращения: 27 ноября 2018. Архивировано 31 мая 2019 года.
- ↑ На Венере обнаружен озоновый слой Архивная копия от 28 ноября 2018 на Wayback Machine, 27 ноября 2018
- ↑ Andrew Dessler. The Chemistry and Physics of Stratospheric Ozone. Academic Press. 2000
См. также
правитьСсылки
править- Озоновый слой Земли. Архивная копия от 24 ноября 2007 на Wayback Machine
- Химия озонового слоя. Архивная копия от 16 февраля 2012 на Wayback Machine
Статьи и обзоры
править- Озон в атмосфере. Озоновый слой — ультрафиолетовый щит Земли
- Химия и алхимия озонового слоя Архивная копия от 14 февраля 2008 на Wayback Machine
- Охрана озонового слоя в мире