Титанат калия
Титанат калия — неорганическое соединение, соль калия и метатитановой кислоты с формулой K2TiO3, бесцветные кристаллы, растворяется в воде с гидролизом, образует кристаллогидрат.
| Титанат калия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
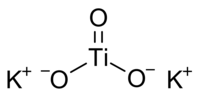
Титанат калия |
| Традиционные названия | Титановокислый калий; метатитанат калия |
| Хим. формула | K2TiO3 |
| Физические свойства | |
| Состояние | бесцветные кристаллы |
| Молярная масса | 174,06 г/моль |
| Плотность | 3,1; 3,58 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 816; 1515 °C |
| Энтальпия | |
| • образования | -1608 кДж/моль |
| Классификация | |
| Рег. номер CAS | 12030-97-6, 39284-88-3 |
| PubChem | 46234667 |
| Рег. номер EINECS | 234-748-6 |
| SMILES | |
| InChI | |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение править
- Сплавление оксида титана с поташем:
- Кипячение титановой кислоты в избытке (для подавления гидролиза) гидроксида калия:
Физические свойства править
Титанат калия образует бесцветные кристаллы ромбической сингонии, пространственная группа C mcm, параметры ячейки a = 1,00283 нм, b = 0,69346 нм, c = 0,54534 нм, Z = 4. Есть данные о тетрагональной ячейке, параметры ячейки a = 0,547 нм, c = 1,1660 нм. Титанат калия растворим в воде.
Химические свойства править
Водный раствор титаната калия неустойчив, и со временем соединение разлагается вследствие гидролиза на титановую кислоту, представляющую собой гидратированный диоксид титана переменного состава, и гидроксид калия. Для ускорения процесса через раствор можно пропустить углекислый газ:
Восстановление титаната калия водородом приводит к образованию титановых бронз состава NaxTiO2 (x = 0.20-0.25). Они представляют собой кристаллические порошки иссиня-чёрного цвета, обладают металлическим блеском и металлической проводимостью.
Титанат калия образует кристаллогидраты состава K2TiO3•4H2O.
Литература править
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1995. — Т. 4. — 639 с. — ISBN 5-82270-092-4.
- CRC Handbook of Chemistry and Physics. — 89th Edition. — Taylor and Francis Group, LLC, 2008-2009.
- Титановый ангидрид // Энциклопедический словарь Брокгауза и Ефрона : в 86 т. (82 т. и 4 доп.). — СПб., 1890—1907.
- Неорганическая химия / под ред. Ю.Д. Третьякова. — М.: Академия, 2007. — Т. 3. — 352 с.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |