Вирусовыделение, или высвобождение вируса из клетки-хозяина — выброс и высвобождение потомства вируса после успешного размножения в клетке-хозяине. После того, как репликация была завершена и клетка-хозяин исчерпала все ресурсы при создании вирусного потомства, вирусы могут начинать покидать клетку несколькими способами[1].
Термин используется для обозначения выделения вируса из одной клетки, также, для обозначения выделения вируса из одной части тела в другую часть тела[2], также, для обозначения выделения из организма в окружающую среду, где вирусы могут заразить другие тела[3].
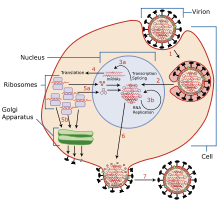
Через почкование
править«Почкование» через клеточную оболочку — по сути, заимствование клеточной мембраны для создания собственной вирусной оболочки — наиболее встречающийся способ размножения тех вирусов, которым в первую очередь нужна оболочка. К таковым относятся вирусы с оболочкой, такие как вирус иммунодефицита человека, вирус простого герпеса первого типа, тяжёлый острый респираторный синдром и натуральная оспа. В начале процесса почкования капсид, — внешняя оболочка вируса, состоящая из белков, — взаимодействует с определенной областью мембраны клетки-хозяина. Во время этого взаимодействия гликозилированный белок вирусной оболочки внедряется в клеточную мембрану. Чтобы успешно расплодиться из клетки-хозяина, капсид вируса должен образовать связь с цитоплазматическими хвостами белков оболочки[4]. Хотя почкование не приводит к немедленному разрушению клетки-хозяина, этот процесс будет медленно истощать клеточную мембрану и в конечном итоге приведет к гибели клетки. Этот процесс также вовлекает противовирусное реагирование, обнаруживающее зараженные вирусом клетки[5]. Почкование наиболее интенсивно изучалось в отношении вирусов из домена эукариоты. Однако было продемонстрировано, что вирусы, инфицирующие прокариоты домена Археи, также используют этот механизм высвобождения вирионов[6].
Через апоптоз
правитьЖивотные клетки запрограммированы на самоуничтожение, когда они подвергаются вирусной атаке или повреждаются каким-либо иным способом. Заставляя клетку подвергаться апоптозу, или самоубийству клетки, вирусное высвобождение потомства в межклеточное пространство становится возможным. Однако апоптоз не обязательно приводит к тому, что клетка просто раскрывается и выливает свое содержимое во межклеточное пространство, — апоптоз обычно контролируется и приводит к тому, что клеточный геном расщепливается до тех пор, пока апоптотические тела (в английской литературе: apoptotic bodies, bleb, — везикулярный нарост плазмы или ядерной мембраны) материала мертвой клетки не оторвутся от клетки, чтобы быть поглощенными макрофагами. Для вируса это хороший способ проникнуть в макрофаги, как для того, чтобы заразить их, так и для того, чтобы таким простым образом путешествовать в другие ткани организма. Хотя этот процесс в основном используется вирусами без оболочки, вирусы с оболочкой также могут его использовать. Вирус иммунодефицита человека является примером вируса с оболочкой, который использует этот процесс для заражения макрофагов[7].
Через экзоцитоз
правитьВирусы также покидают клетки через экзоцитоз, которого клетка-хозяин не разрушается. Вирусы, которые относятся к вирусам с оболочками из ядерных или эндосомальных мембран могут покинуть клетку через экзоцитоз[4]. Вирусное потомство синтезируется в клетке, и транспортная система клетки-хозяина используется для включения их в везикулы; везикулы вирусного потомства переносятся на клеточную мембрану и затем высвобождаются во межнеклеточное пространство. Это используется, прежде всего, вирусами без оболочки, хотя вирусы с оболочкой также показывают это. Примером является использование рециркуляции рецепторов вирусных частиц вирусом ветряной оспы, имеющей оболочку[8].
Контагиозность
правитьЧеловек с вирусным заболеванием заразен, если он выделяет вирусы. Поэтому скорость, с которой зараженный человек с течением определённого времени выделяет вирусы, представляет значительный интерес. Некоторые вирусы, такие как Вирус простого герпеса первого типа (который вызывает генитальный герпес), могут вызывать «бессимптомное выделение вируса» и, следовательно, распространяться незамеченными от человека к человеку, так как при этом нет повышенной температуры и других признаков болезни, которые бы показали контагиозную природу хозяина во время такого рода вирусовыделения[9].
Другим важным компонентом вирусовыделения является вопрос о том, играет ли возраст зараженного человека роль в том, как долго человек будет распространять вирус. Миланский университет провел исследование вируса гриппа A/H1N1/2009, чтобы определить, происходит ли распространение новой пандемии в течение более длительного времени у молодых, чем у взрослых. В исследование были включены только дети с симптомами, которые появились за два дня до посещения больницы, они были моложе 15 лет и не сталкивались с какими-либо серьезными осложнениями. После физических осмотров и образцов, взятых из глотки детей с вирусоположительным диагнозом, результаты определили, что продолжительность вирусовыделения (в днях) не зависит от возраста. Вирусовыделение не было связано с возрастом, потому что не было различий между детьми в разных возрастных группах. Заразность в этой ситуации может длиться до 15 дней, что означает, что, когда данное вирусное заболевание поражает большую часть локализованной популяции, должны быть приняты надлежащие меры карантинной защиты, чтобы предотвратить дальнейшее распространение вируса через вирусовыделение[10].
См. также
правитьПримечания
править- ↑ Introduction to Modern Virology 6th Edition. by Nigel J. Dimmock (Author), Andrew J. Easton (Author), Keith N. Leppard (Author). Wiley-Blackwell; 6 edition (January 16, 2007) ISBN 978-1405136457
- ↑ [1] Архивная копия от 20 апреля 2020 на Wayback Machine Massachusetts Department of Public Health — Rabies Control Plan — Chapter 1: General Information — «Definitions as Used in this Document […] Shedding — The release of rabies virus from the salivary glands into the saliva.»
- ↑ Hall CB, Douglas RG, Geiman JM, Meagher MP (October 1979). "Viral shedding patterns of children with influenza B infection". The Journal of Infectious Diseases. 140 (4): 610—3. doi:10.1093/infdis/140.4.610. PMID 512419.
- ↑ 1 2 Payne, Susan (2017). "Virus Interactions With the Cell". Viruses: 23-25. Архивировано 30 июля 2019. Дата обращения: 7 апреля 2020.
- ↑ Pornillos O, Garrus JE, Sundquist WI (December 2002). "Mechanisms of enveloped RNA virus budding". Trends in Cell Biology. 12 (12): 569—79. doi:10.1016/s0962-8924(02)02402-9. PMID 12495845.
- ↑ Quemin ER, Chlanda P, Sachse M, Forterre P, Prangishvili D, Krupovic M (September 2016). "Eukaryotic-Like Virus Budding in Archaea". mBio. 7 (5). doi:10.1128/mBio.01439-16. PMC 5021807. PMID 27624130.
- ↑ Stewart SA, Poon B, Song JY, Chen IS (April 2000). "Human immunodeficiency virus type 1 vpr induces apoptosis through caspase activation". Journal of Virology. 74 (7): 3105—11. doi:10.1128/jvi.74.7.3105-3111.2000. PMC 111809. PMID 10708425.
- ↑ Olson JK, Grose C (May 1997). "Endocytosis and recycling of varicella-zoster virus Fc receptor glycoprotein gE: internalization mediated by a YXXL motif in the cytoplasmic tail". Journal of Virology. 71 (5): 4042—54. PMC 191557. PMID 9094682.
- ↑ Daniel J., DeNoon Genital Herpes' Silent Spread. WebMD. Дата обращения: 29 января 2019. Архивировано 29 января 2019 года.
- ↑ Esposito, Susanna; Daleno, Cristina; Baldanti, Fausto; Scala, Alessia; Campanini, Giulia; Taroni, Francesca (2011-07-13). "Viral shedding in children infected by pandemic A/H1N1/2009 influenza virus". Virology. 8. Дата обращения: 7 апреля 2020.
{{cite journal}}: Википедия:Обслуживание CS1 (url-status) (ссылка)