Гексафтороалюминат натрия
Гексафтороалюминат натрия — неорганическое вещество, смешанная соль плавиковой кислоты и металлов алюминия и натрия, с формулой Na3[AlF6]. Бесцветные кристаллы, плохо растворимые в воде.
| Гексафтороалюминат натрия | |
|---|---|
 | |
| Общие | |
| Систематическое наименование |
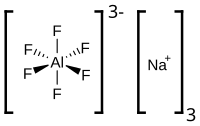
Гексафтороалюминат натрия |
| Традиционные названия | Фтористый алюминий-натрий |
| Хим. формула | Na3[AlF6] |
| Физические свойства | |
| Состояние | Бесцветные кристаллы |
| Молярная масса | 209,94 г/моль |
| Плотность | 2,89; 2,90; 2,97 г/см³ |
| Термические свойства | |
| Температура | |
| • плавления | 1000; 1011 °C |
| Мол. теплоёмк. | 216 Дж/(моль·К) |
| Энтальпия | |
| • образования | -3312 кДж/моль |
| Давление пара | 0 ± 1 мм рт.ст.[1] |
| Химические свойства | |
| Растворимость | |
| • в воде | 0,04 г/100 мл |
| Оптические свойства | |
| Показатель преломления | 1,3389 |
| Классификация | |
| Рег. номер CAS | 13775-53-6 |
| PubChem | 16693908 |
| Рег. номер EINECS | 237-410-6 |
| SMILES | |
| InChI | |
| RTECS | WA9625000 |
| ChEBI | 39289 |
| ChemSpider | 11431435 и 140411 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Получение
править- В природе встречается редкий минерал криолит из группы природных фторидов, химический состав Na3[AlF6] с незначительными примесями.
- Из насыщенных растворов фторидов натрия и алюминия:
- Действием плавиковой кислоты на гидроксид алюминия и фторид натрия:
- Обменными реакциями:
Физические свойства
правитьГексафтороалюминат натрия образует бесцветные кристаллы моноклинной сингонии, пространственная группа P 21/n, параметры ячейки a = 0,780 нм, b = 0,561 нм, c = 0,546 нм, β = 90,18°, Z = 2.
Расплав гексафтороалюмината натрия является электролитом и проводит электрический ток.
Химические свойства
править- В расплаве диссоциирует:
- При дальнейшем нагревании начинает разлагаться:
- Разлагается концентрированными кислотами:
- и щелочами:
Применение
править- Компонент электролита при производстве алюминия.
- Металлургический флюс.
- Компонент стёкол и эмалей.
- Наполнитель для резины.
- Относится к многотоннажному производству, цена технического продукта ~1000$/т, чистого ~6$/кг.
Примечания
правитьЛитература
править- Лидин Р.А. и др. Химические свойства неорганических веществ: Учеб. пособие для вузов. — 3-е изд., испр. — М.: Химия, 2000. — 480 с. — ISBN 5-7245-1163-0.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Справочник химика / Редкол.: Никольский Б.П. и др.. — 2-е изд., испр. — М.—Л.: Химия, 1966. — Т. 1. — 1072 с.
- Рипан Р., Четяну И. Неорганическая химия. Химия металлов. — М.: Мир, 1971. — Т. 1. — 561 с.
Это заготовка статьи о неорганическом веществе. Помогите Википедии, дополнив её. |