Дистилляция
Дистилля́ция (от лат. distillatio — стекание каплями; перегонка) — процесс испарения жидкости с последующим охлаждением и конденсацией паров, который используется, прежде всего, для разделения жидких смесей и очистки выделяемых веществ. Основан на различии в температурах кипения компонентов смеси. В зависимости от состава разделяемой смеси и целей процесса, продуктами дистилляции могут быть как дистиллят (отогнанные фракции), обогащённый более летучими (низкокипящими) компонентами, так и неотогнанный (кубовый) остаток, содержащий менее летучие (высококипящие) компоненты[1][2].
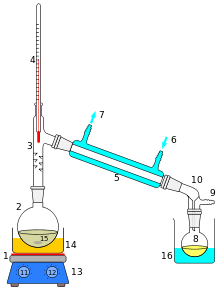
1 Нагревательный элемент
2 Перегонный куб
3 Насадка Вюрца с дефлегматором
4 Термометр
5 Холодильник
6 Подвод охлаждающей жидкости
7 Отвод охлаждающей жидкости
8 Приёмная колба
9 Отвод газа (в том числе при пониженном давлении)
10 Аллонж
11 Регулятор температуры нагревателя
12 Регулятор скорости перемешивания
13 Магнитная мешалка
14 Водяная (масляная, песочная и т. п.) баня
15 Мешалка или центры кипения
16 Охлаждающая ванна
Различают дистилляцию с конденсацией пара в жидкость (при которой получаемый дистиллят имеет усреднённый состав вследствие перемешивания) и дистилляцию с конденсацией пара в твёрдую фазу (при которой в конденсате возникает распределение концентрации компонентов).
Основными деталями дистилляционного устройства являются испаритель, представляющий собой обогреваемый контейнер (куб) для перегоняемой жидкости, дефлегматор, для частичной конденсации пара, выходящего из испарителя, охлаждаемый конденсатор (холодильник), сборник дистиллята и соединяющий их паропровод[1][2].
Дистилляция применяется в промышленности и в лабораторной практике для разделения и рафинирования сложных веществ: для разделения смесей органических веществ (например, разделение нефти на бензин, керосин, дизельное топливо и др.; получение душистых веществ в парфюмерии; очистка этилового спирта) и для получения высокочистых неорганических веществ (например, металлов: бериллия, свинца, цинка, магния, кадмия, ртути; и неметаллов: серы, селена и др.).
Теория дистилляции править
В теории дистилляции в первую очередь рассматривается разделение смесей двух веществ[2]. Принцип дистилляции основан на том, что концентрация некоторого компонента в жидкости отличается от его концентрации в паре этой жидкости. Отношение = является характеристикой процесса и называется коэффициентом разделения (или распределения) при дистилляции. (Также коэффициентом разделения при дистилляции называют величину ). Коэффициент разделения зависит от природы разделяемых компонентов и условий дистилляции. В зависимости от условий дистилляции различают идеальный (определяемый только парциальными давлениями паро́в чистых компонентов), равновесный (когда число частиц, покидающих в единицу времени жидкость, равно числу частиц, возвращающихся в это же время в жидкость) и эффективный коэффициенты разделения. Практически дистилляция веществ сильно зависит от интенсивности перемешивания жидкости, а также от взаимодействия примесей с основным компонентом и с другими примесными компонентами с образованием соединений (в связи с чем дистилляция считается физико-химическим процессом). Эффективный коэффициент разделения смеси «основное вещество — примесь» может на несколько порядков отличаться от идеального коэффициента разделения.
Режимы дистилляции характеризуются температурой испарения и степенью отклонения от фазового равновесия жидкость-пар. Обычно в дистилляционном процессе , где — число частиц вещества, переходящих в единицу времени из жидкости в пар, — число частиц, возвращающихся в это же время из пара в жидкость, — число частиц, переходящих в это время в конденсат. Отношение является показателем отклонения процесса от равновесного. Предельными являются режимы, в которых (равновесное состояние системы жидкость-пар) и (режим молекулярной дистилляции).
Идеальный коэффициент разделения двухкомпонентного вещества может быть выражен через давления и чистых компонентов при температуре процесса: . С учётом коэффициентов активности компонентов и , отражающих взаимодействие компонентов в жидкости, коэффициент разделения . Коэффициенты активности имеют температурную и концентрационную зависимости (см. активность (химия)). С понижением температуры значение коэффициента разделения обычно удаляется от единицы, то есть эффективность разделения при этом увеличивается.
При все испаряющиеся частицы переходят в конденсат (режим молекулярной дистилляции). В этом режиме коэффициент разделения , где и — молекулярные массы первого и второго компонентов соответственно. Определение молекулярного режима дистилляции возможно по величине , где — расстояние от испарителя до конденсатора, — длина свободного пробега молекул дистиллируемого вещества, — константа, зависящая от конструкции аппарата. При наблюдается молекулярное испарение, при между жидкостью и паром устанавливается динамическое равновесие, а при других значениях испарение имеет промежуточный характер. Режим молекулярной дистилляции может применяться в различных дистилляционных способах, включая ректификацию. Обычно молекулярная дистилляция осуществляется в вакууме при низком давлении пара и при близком расположении поверхности конденсации к поверхности испарения (что исключает столкновение частиц пара друг с другом и с частицами атмосферы). В режиме, близком к молекулярной дистилляции, проводится дистилляция металлов. В связи с тем, что коэффициент разделения при молекулярной дистилляции зависит не только от парциальных давлений компонентов, но и от их молекулярных (или атомных) масс, молекулярная дистилляция может применяться для разделения смесей, для которых , — азеотропных смесей, включая смеси изотопов.
В общем случае, математическое описание дистилляции (и сублимации) представляется в виде системы уравнений, содержащих два параметра: эффективный коэффициент разделения β и диффузионное число Пекле Ре=w(T)X / ρD(T), где w - скорость испарения вещества с единицы поверхности; D - коэффициент диффузии примеси; X - размерный фактор испаряемого материала (например, толщина слоя испаряемого материала); ρ - плотность вещества. Ввиду сложности уравнений, их решение может быть найдено только численными методами. В простом случае, когда дистилляция осуществляется в условиях интенсивного перемешивания испаряемой жидкости (и конденсата), когда Ре=0 или мало, уравнения, связывающие содержание второго компонента в конденсате и в остатке с долей перегонки или с долей остатка при заданных условиях процесса и известной начальной концентрации жидкости ( , и — масса конденсата и остатка, а также начальная масса дистиллируемого вещества соответственно), имеют простой вид с одним параметром β.
При дистилляции вещества с большой концентрацией компонентов (с конденсацией пара в жидкость), при несильной зависимости коэффициентов активности компонентов от их концентраций взаимосвязь величин , и , когда используются концентрации в процентах, имеет вид:
Для дистилляции с конденсацией пара в жидкость при малом содержании примеси
- =
где — коэффициент разделения.
Также выведены уравнения распределения компонентов в твёрдом конденсате, получаемого дистилляцией с направленным затвердеванием конденсата или зонной дистилляцией.
Отмечено, что дистилляционные уравнения описывают не только процессы распределения компонентов в системах "жидкость - пар", но и в других контактирующих фазах (например, переходы "жидкий кристалл - кристалл", "жидкий кристалл-жидкость", "газ - плазма", а также переходы, связанные с квантово-механическими состояниями — сверхтекучая жидкость, конденсат Бозе — Эйнштейна) — при подстановке в них соответствующих коэффициентов разделения.
Дистилляция с конденсацией пара в жидкость править
Простая перегонка — частичное испарение жидкой смеси путём непрерывного отвода и конденсации образовавшихся паров в холодильнике. Полученный конденсат называется дистиллятом, а неиспарившаяся жидкость — кубовым остатком.
Фракционная дистилляция (или дробная перегонка) — разделение многокомпонентных жидких смесей на отличающиеся по составу части, фракции, путём сбора конденсата частями с различной летучестью, начиная с первой, обогащенной низкокипящим компонентом. Остаток жидкости обогащён высококипящим компонентом. Для улучшения разделения фракций применяют дефлегматор.
Ректификация — способ дистилляции, при котором часть жидкого конденсата (флегма) постоянно возвращается в куб, двигаясь навстречу пару в колонне. В результате этого примеси, содержащиеся в паре, частично переходят во флегму и возвращаются в куб, при этом чистота пара (и конденсата) повышается.
Дистилляция с конденсацией пара в твёрдую фазу править
Дистилляция с конденсацией пара в градиенте температуры — дистилляционный процесс, в котором конденсация в твёрдую фазу осуществляется на поверхности, имеющей градиент температуры, с многократным реиспарением частиц пара. Менее летучие компоненты осаждаются при более высоких температурах. В результате в конденсате возникает распределение примесей вдоль температурного градиента, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Разделение компонентов пара при реиспарении подчиняется собственным закономерностям. Так, при молекулярной дистилляции соотношение между количествами и осаждённых в конденсаторе первого и второго компонентов, соответственно, выражается равенством:
где и — скорости испарения первого компонента из расплава и с поверхности реиспарения соответственно, и — то же для второго компонента, и — коэффициенты конденсации первого и второго компонентов соответственно, — коэффициент, зависящий от поверхности испарения и углов испарения и реиспарения. Реиспарение повышает эффективность очистки от трудноудаляемых малолетучих примесей в 2—5 раз, а от легколетучих — на порядок и более (по сравнению с простой перегонкой). Этот вид дистилляции нашёл применение в промышленном производстве высокочистого бериллия.
Дистилляция с направленным затвердеванием конденсата (дистилляция с вытягиванием дистиллята) — дистилляционный процесс в контейнере удлинённой формы c полным расплавлением дистиллируемого вещества и конденсацией пара в твёрдую фазу по мере вытягивания конденсата в холодную область. Процесс разработан теоретически.
В получаемом конденсате возникает неравномерное распределение примесей, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Процесс является дистилляционным аналогом нормальной направленной кристаллизации. Распределение примеси в конденсате описывается уравнением:
где — концентрация примеси в дистилляте на расстоянии от начала, — высота конденсата при полностью испарившемся дистиллируемом материале.
Зонная дистилляция — дистилляционный процесс в контейнере удлинённой формы c расплавлением только верхней части рафинируемого вещества в перемещаемой вниз жидкой зоне, с конденсацией пара в твёрдую фазу по мере выхода конденсата в холодную область. Процесс разработан теоретически.
При движении зонного нагревателя вдоль контейнера сверху вниз в контейнере формируется твёрдый конденсат с неравномерным распределением примесей, и наиболее чистая часть конденсата может быть выделена в качестве продукта. Процесс может быть повторён многократно, для чего конденсат, полученный в предыдущем процессе, должен быть перемещён (без переворота) в нижнюю часть контейнера на место рафинируемого вещества. Неравномерность распределения примесей в конденсате (то есть эффективность очистки) растёт с увеличением числа повторений процесса.
Зонная дистилляция является дистилляционным аналогом зонной перекристаллизации. Распределение примесей в конденсате описывается известными уравнениями зонной перекристаллизации с заданным числом проходов зоны — при замене коэффициента распределения для кристаллизации на коэффициент разделения для дистилляции. Так, после одного прохода зоны
где — концентрация примеси в конденсате на расстоянии от начала конденсата, — длина жидкой зоны.
Специальные приёмы дистилляции править
Эффективность дистилляционной очистки может быть повышена введением в систему основа-примесь добавочного компонента (обычно в концентрации 0,5…10 %), который изменяет относительную летучесть примеси. Разновидностью данного метода (экстрактивная дистилляция) является дистилляция в атмосфере активного вещества, прежде всего — водяного пара.
Применяются и другие специальные приёмы повышения эффективности однократной дистилляции — такие как горячий конденсатор, конденсатор с градиентом температуры, создание на поверхности испаряемой жидкости слоя оксида.
Отмечается, что эффективность применения специальных приёмов дистилляции зависит от величины идеального коэффициента разделения в дистиллируемой двойной системе: она меньше в системах, для которых идеальный коэффициент разделения ближе к единице.
История править
Дистиллированная вода была известна как минимум с 200 г. н. э., когда Александр Афродисий описал процесс её изготовления[3]. В принципе ещё Аристотель, описывая в трактате «Метеорология» очистку морской воды путём испарения, по сути ведёт речь о дистилляции[4]. Первые сведения о перегонке этилового спирта относятся к рубежу нашей эры и происходят от греческих алхимиков из Александрии[5]. Практически одновременно перегонка спирта стала известна в китайской империи Хань[6]. В XI веке, у Авиценны, дистилляция упоминается как метод получения эфирных масел. C середины XIX века разрабатывается ректификация. Подробнее см. История дистилляции спирта.
См. также править
Примечания править
- ↑ 1 2 Коган В.Б. Дистилляция // Химическая энциклопедия : в 5 т. / Гл. ред. И. Л. Кнунянц. — М.: Советская энциклопедия, 1990. — Т. 2: Даффа — Меди. — С. [84—87] (стб. 159—165). — 671 с. — 100 000 экз. — ISBN 5-85270-035-5.
- ↑ 1 2 3 Дистилляция / В. Л. Пебалк // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.
- ↑ Taylor, F. Sherwood The Evolution of the Still (англ.) // Annals of Science : journal. — 1945. — Vol. 5, no. 3. — P. 186. — ISSN 0003-3790. — doi:10.1080/00033794500201451.
- ↑ Heather Greene. Distilling 101: How Whiskey Is Actually Made (англ.). Eater (4 января 2016). Дата обращения: 10 сентября 2022. Архивировано 10 сентября 2022 года.
- ↑ Forbes, Robert James. A short history of the art of distillation: from the beginnings up to the death of Cellier Blumenthal (англ.). — BRILL, 1970. — ISBN 978-90-04-00617-1. Архивировано 23 января 2023 года.
- ↑ Marco Polo's China: A Venetian in the Realm of Khubilai Khan - Stephen G. Haw - Google Books
Литература править
- Дытнерский Ю. И. Процессы и аппараты химической технологии: Учебник для вузов. Изд. 2. В 2-х кн. Часть 2. Массообменные процессы и аппараты. М.: Химия, 1995. — 368 с.
- King C.J. Separation processes – Second edition, N.Y.: Dover Publication. 2013. (835 p.)
- Гельперин Н. И. Основные процессы и аппараты химической технологии. — М.: Химия, 1981. — 812 с.
- Девятых Г. Г., Еллиев Ю. Е. Введение в теорию глубокой очистки веществ. — М.: Наука, 1981. — 320 с.
- Девятых Г. Г., Еллиев Ю. Е. Глубокая очистка веществ. — М.: Высшая школа, 1990. — 192 с.
- Емельянов В. С., Евстюхин А. И., Шулов В. А. Теория процессов получения чистых металлов, сплавов и интерметаллидов. — М.: Энергоатомиздат, 1983. — 144 с.
- Жаров В. Т., Серафимов Л. А. Физико-химические основы дистилляции и ректификации. — Л.: Химия, 1975. — 240 с.
- Степин Б. Д., Горштейн И. Г., Блюм Г. З., Курдюмов Г. М., Оглоблина И. П. Методы получения особо чистых неорганических веществ. — Л.: Химия, 1969. — 480 с.
- Сийрде Э. К., Теаро Э. Н., Миккал В. Я. Дистилляция. — Л.: Химия, 1971. — 216 с.
- Калашник О. Н., Нисельсон Л. А. Очистка простых веществ дистилляцией с гидротермальным окислением примесей // Высокочистые вещества, 1987. — № 2. — С. 74—78.
- Корякин Ю. В., Ангелов И. И. Чистые химические вещества. Руководство по приготовлению неорганических реактивов и препаратов в лабораторных условиях. — М.: Химия, 1974.
- Беляев А. И. Физико-химические основы очистки металлов и полупроводниковых веществ. — М.: Металлургия, 1973. — 224 с.
- Нисельсон Л. А., Лапин Н. В., Бежок В. С. Определение относительных летучестей примесей в жидком германии // Высокочистые вещества, 1989. — N. 6. — С. 33—38 [Содержатся сведения о коэффициенте f скорости испарения вещества — со ссылкой на: Borrows G. // Trans. Inst. Chem. Eng., 1954. — V. 32. — P. 23.]
- Пазухин В. А., Фишер А. Я. Разделение и рафинирование металлов в вакууме. — М.: Металлургия, 1969. — 204 с.
- Иванов В. Е., Папиров И. И., Тихинский Г. Ф., Амоненко В. М. Чистые и сверхчистые металлы (получение методом дистилляции в вакууме). — М.: Металлургия, 1965. — 263 с.
- Несмеянов А. Н. Давление пара химических элементов. — М.: Издательство АН СССР, 1961. — 320 с.
- Есютин В. С., Нургалиев Д. Н. Вакуум-дистилляционная очистка свинца от примесей в аппарате непрерывного действия // Цветные металлы, 1975. — № 12. — С. 28-30.
- Кравченко А. И. О временной зависимости состава двойного сплава при его разгонке в вакууме // Известия АН СССР. Серия: Металлы. — 1983. — № 3. — С. 61—63.
- Кравченко А. И. Об уравнениях дистилляции при малом содержании примеси // Вопросы атомной науки и техники, 1990. — № 1 — Серия: «Ядерно-физические исследования» (9). — С. 29—30.
- Нисельсон Л. Я., Ярошевский А. Г. Межфазовые коэффициенты распределения (Равновесия кристалл-жидкость и жидкость-пар). — М.: Наука, 1992. — 399 с.
- Kravchenko A.I. Simple substances refining: efficiency of distillation methods // Functional Materials, 2000 — V. 7. — N. 2. — P. 315—318.
- Кравченко А. И. Уравнение распределения примеси в твёрдом дистилляте // Неорганические материалы, 2007. — Т. 43. — № 8. — С. 1021—1022.
- Кравченко А. И. Эффективность очистки в дистилляционном и кристаллизационном процессах // Неорганические материалы, 2010. — Т. 46. — № 1. — С. 99—101.
- Кравченко А. И. Дистилляция с вытягиванием дистиллята // Вопросы атомной науки и техники, 2008. — № 1 — Серия: «Вакуум, чистые материалы, сверхпроводники» (17). — С. 18—19. [1]
- Кравченко А. И. Зонная дистилляция // Вопросы атомной науки и техники, 2011. — № 6 — Серия: «Вакуум, чистые материалы, сверхпроводники» (19). — С. 24—26. [2]
- Кравченко А. И. Разработка перспективных схем зонной дистилляции // Перспективные материалы, 2014. — № 7. — С. 68-72. [www.j-pm.ru].
- Кравченко А. И. О распределении примесей при фазовых переходах из фазы с идеальным перемешиванием // Вопросы атомной науки и техники, 2011. — № 6 — Серия: «Вакуум, чистые материалы, сверхпроводники» (19). — С. 27—29. [3]
- Папиров И. И., Кравченко А. И., Мазин А. И., Шиян А. В., Вирич В. Д. Распределение примесей в сублимате магния // Неорганические материалы, 2015. — Т. 51. — № 6. — С. 625—627.
- Кириллов Ю. П., Кузнецов Л. А., Шапошников В. А. , Чурбанов М. Ф. Влияние диффузии на глубину очистки веществ дистилляцией // Неорганические материалы, 2015. — Т. 51. — № 11. — С. 1177—1189.
- Кравченко А. И. Соотношение между эффективным и идеальным коэффициентами разделения при дистилляции и сублимации // Неорганические материалы, 2016. — Т. 52. — № 4. — С. 423—430.
- Кириллов Ю. П., Шапошников В. А. , Кузнецов Л. А., Ширяев В. С. , Чурбанов М. Ф. Моделирование испарения жидких веществ и конденсации их паров при дистилляции // Неорганические материалы, 2016. — Т. 52. — № 11. — С. 1256—1261.
- Кравченко А. И. О температурной зависимости идеального коэффициента разделения в системах с близкой летучестью компонентов // Вопросы атомной науки и техники, 2016. — № 1 — Серия: «Вакуум, чистые материалы, сверхпроводники» (21). — С. 14—16.
- Папиров И. И., Кравченко А. И., Мазин А. И., Шиян А. В., Вирич В. Д. Распределения примесей в сублиматах магния // Вопросы атомной науки и техники, 2016. — № 1 — Серия: «Вакуум, чистые материалы, сверхпроводники» (21). — С. 21—22.
- Жуков А. И., Кравченко А. И. Расчёт сублимации с учётом диффузии примеси // Неорганические материалы, 2017. — Т. 53. — № 6. — С. 662—668.
- Кравченко А. И. О рафинировании простых веществ дистилляцией с добавочным компонентом // Вопросы атомной науки и техники, 2018. — № 1 — Серия: «Вакуум, чистые материалы, сверхпроводники» (22). — С. 9—13.
- Кравченко А. И. Расчёт дистилляционного рафинирования вещества с легколетучей и труднолетучей примесями // Неорганические материалы, 2018. — Т. 54. — № 5. — С. 520—522.
- Кравченко А. И. Эффективность многократного дистилляционного или кристаллизационного рафинирования с заданным выходом // Неорганические материалы, 2020. — Т. 56. — № 10. — С. 1112-1116.
- Кравченко А. И., Жуков А.И. Температурная зависимость числа Пекле в процессах сублимации простых веществ // Неорганические материалы, 2021. — Т. 57. — № 7. — С. 789-795.
- Xiaoxin Zh., Semiramis F., Bernd F. Separation behavior of arsenic and lead from antimony during vacuum distillation and zone refining // Journal of Materials Research and Technology, 2020. V. 9. Is. 3. P. 4386-4398. [Дистилляция и зонная плавка сурьмы с добавочными компонентами Al и Zn.]
- Кравченко А. И. Критерии применимости многократного дистилляционного или кристаллизационного рафинирования взамен однократного при заданных производительности и выходе // Неорганические материалы, 2021. — Т. 57. — № 7. — С. 783-788.
- Кравченко А. И., Жуков А.И. Коэффициенты разделения и числа Пекле в испарительных процессах рафинирования веществ с простой основой при температурах вблизи от температур плавления // Неорганические материалы, 2022. — Т. 58. — № 8. — С. 891-896.
- Zhukov A.I., Kravchenko A.I. Calculation of distribution of impurities in solidified condensate into account of Peclet number // Problems of atomic science and technology, 2024. N. 1. P. 25-28. https://doi.org/10.46813/2024-149-025
- Kravchenko A.I. On theory of evaporation refining // Problems of atomic science and technology, 2024. N. 1. P. 33-34. https://doi.org/10.46813/2024-149-033
- Kravchenko A.I. Evaluating the efficiency of evaporation refining using the Burton-Prim-Slichter equation // Problems of atomic science and technology, 2024. N. 1. P. 35-37. https://doi.org/10.46813/2024-149-035
- ГОСТ 2177—99 (ASTM D86). Нефтепродукты. Методы определения фракционного состава.