Водородная связь
Водородная связь — форма ассоциации между электроотрицательным атомом и атомом водорода H, связанным ковалентно с другим электроотрицательным атомом. Характерными примерами таких электроотрицательных атомов являются атомы элементов второго периода периодической системы — азота, кислорода и фтора, а также атомы некоторых других элементов с высокой относительно водорода электроотрицательностью. Водородные связи могут быть межмолекулярными или внутримолекулярными[1].
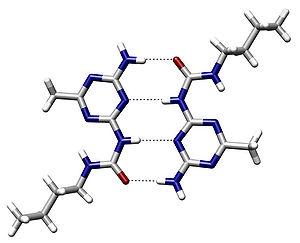
Природа править
Ранее водородную связь рассматривали как электростатическое взаимодействие, усиленное небольшим размером водорода, которое разрешает близость взаимодействующих диполей. Тогда об этом говорят как о разновидности донорно-акцепторной связи, невалентном взаимодействии между атомом водорода H, ковалентно связанным с атомом A группы A–H молекулы RA–H и электроотрицательным атомом B другой молекулы BR' (или функциональной группы той же молекулы). Результатом таких взаимодействий являются комплексы RA–H···BR′ различной степени стабильности, в которых атом водорода выступает в роли «моста», связывающего фрагменты RA и BR′[2].
Особенностями водородной связи, по которым её выделяют в отдельный вид, является её не очень высокая прочность[3], её распространенность и важность, особенно в органических соединениях[4], а также некоторые побочные эффекты, связанные с малыми размерами и отсутствием дополнительных электронов у водорода.
В настоящее время с развитием квантовохимических расчетов в рамках теории молекулярных орбиталей водородная связь рассматривается как частный случай ковалентной с делокализацией электронной плотности по цепи атомов и образованием трёхцентровых четырёхэлектронных связей (например, –H···[F–H···F]–) или даже четырехцентровых пятиэлектронных связей (в случае образования бифуркатных связей ).
История править
В книге The Nature of Chemical Bond and the Structure of Molecules and Crystals Лайнуса Полинга, впервые изданной в 1939 году, первое упоминание водородной связи приписывается Муру и Винмиллу. Они использовали водородную связь, чтобы обосновать факт, что гидроксид триметиламмония является более слабым основанием, чем гидроксид тетраметиламмония.[5] Описание водородных связей в воде было сделано в 1920 году Латимером и Родебушем[6].
Свойства править
Энергия водородной связи значительно меньше энергии обычной ковалентной связи (не превышает 40 кДж/моль для нейтральных комплексов и 160 кДж/моль для ион-молекулярных комплексов). Однако этой энергии достаточно, чтобы вызвать ассоциацию молекул, то есть их объединение в димеры или более крупные кластеры[7]. Именно ассоциация молекул служит причиной аномально высоких температур плавления и кипения таких веществ, как фтороводород, вода, аммиак. Связь этого типа, хотя и слабее ионной и ковалентной связей, играет очень важную роль во внутри- и межмолекулярных взаимодействиях. Водородные связи во многом обусловливают физические свойства воды и многих органических жидкостей (спирты, карбоновые кислоты, амиды карбоновых кислот, сложные эфиры). Прочность водородной связи (энтальпия образования комплекса) зависит от полярности комплекса и колеблется от ~ 6 кДж/моль для комплексов молекул галогеноводородов с инертными газами до 160 кДж/моль для ион-молекулярных комплексов (AHB)±; так, для комплекса (H2O•H•OH2)+, образованного H2O и H3O+ — 132 кДж/моль в газовой фазе.
В воде править
Механизм Гротгуса править
Аномально высокая теплоёмкость воды, а также теплопроводность многоатомных спиртов обеспечивается многочисленными водородными связями. Одна молекула воды может образовать до четырёх классических водородных связей с соседями (с учётом бифуркатных H-связей до 5—6).
Водородные связи повышают температуру кипения, вязкость и поверхностное натяжение жидкостей. Они ответственны за многие другие уникальные свойства воды.
Водные кластеры править
Согласно современным представлениям, наличие водородных связей между молекулами воды приводит к возникновению так называемых водных кластеров или комплексов. Простейшим примером такого кластера может служить димер воды:
Энергия водородной связи в димере воды составляет 0,2 эВ (≈ 5 ккал/моль), что всего на порядок больше, чем характерная энергия теплового движения при температуре 300 К. В то же время энергия ковалентной связи O–H в 200 раз больше тепловой энергии. Таким образом, водородные связи относительно слабы и неустойчивы: предполагается, что они могут легко возникать и исчезать в результате тепловых флуктуаций. Это, в частности, приводит к тому, что вода должна рассматриваться не как «простая», а как «связанная жидкость»: вода представляется как сеть молекул , соединённых водородными связями[8].
В нуклеиновых кислотах и белках править
Водородная связь в значительной мере определяет свойства и таких биологически важных веществ, как белки и нуклеиновые кислоты. В частности, элементы вторичной структуры (например, α-спирали, β-складки) и третичной структуры в молекулах белков, РНК и ДНК стабилизированы водородными связями. В этих макромолекулах водородные связи сцепляют части той же самой макромолекулы, заставляя её сворачиваться в определённую форму. Например, двойная спиральная структура ДНК определяется в значительной степени наличием водородных связей, сцепляющих пары нуклеотидов, которые связывают одну комплементарную нить с другой.
В полимерах править
Многие полимеры усилены водородными связями в их главных цепях. Среди синтетических полимеров самый известный пример — нейлон, где водородные связи играют главную роль в кристаллизации материала. Водородные связи также важны в структуре полученных искусственно полимеров (например, целлюлозы) и в многих различных формах в природе, таких как древесина, хлопок и лён.
В твердом теле править
Для твердого тела в настоящее время разработан математический аппарат - метод расчета и анализа поверхности Хиршфельда, позволяющий точно оценивать вклад водородных связей в межмолекулярные взаимодействия. Применение этого метода позволяет также количественно сравнивать вклады различных типов межмолекулярных взаимодействий друг с другом[9][10].
В биологических системах править
При формировании биологических мембран (особенно фосфолипидных) в клетках водородные связи играют определяющую роль, обеспечивая их векторность (направленность внешней поверхности мембран в сторону водной среды — субстрата).
См. также править
Примечания править
- ↑ Определение по IUPAC. Дата обращения: 5 мая 2011. Архивировано 19 марта 2008 года.
- ↑ Афанасьев А. В., Белова Е.В., Герман К.Э., Новиков А.П. Номенклатура, электронное строение органических соединений и новые подходы к оценке их реакционной способности. — М.: Издательский дом "Граница", 2022. — С. 89-109. — 110 с. — ISBN 978-5-9933-0408-3. Архивировано 17 февраля 2023 года.
- ↑ Энергия связи H···N = 8 кДж/моль, связи H···O — около 21 кДж/моль, связи H···F около 36 кДж/моль [1] Архивная копия от 22 сентября 2011 на Wayback Machine. Для сравнения, энергия ковалентной связи — 400—900 кДж/моль [2] Архивная копия от 18 сентября 2010 на Wayback Machine
- ↑ Например, водородными связями обусловлена форма молекулы ДНК
- ↑ T. S. Moore and T. F. Winmill. The state of amines in aqueous solution (англ.) // J. Chem. Soc.. — 1912. — Vol. 101. — P. 1635—1676. — doi:10.1039/CT9120101635.
- ↑ Wendell M. Latimer, Worth H. Rodebush. POLARITY AND IONIZATION FROM THE STANDPOINT OF THE LEWIS THEORY OF VALENCE. (англ.) // J. Am. Chem. Soc.. — 1920. — Vol. 42. — P. 1419–1433. — doi:10.1021/ja01452a015.
- ↑ Association (англ.). IUPAC Compendium of Chemical Terminology, 3rd ed.. doi:10.1351/goldbook.a00472. Дата обращения: 5 февраля 2024. Архивировано 5 февраля 2024 года.
- ↑ Dominik Marx. Proton Transfer 200 Years after von Grotthuss: Insights fromAb Initio Simulations (англ.) // ChemPhysChem. — 2006. — Vol. 7. — P. 1848—1870. — doi:10.1002/cphc.200600128.
- ↑ K. A. Zagidullin, A. P. Novikov, D. A. Zelenina, M. S. Grigoriev, K. E. German. Synthesis, crystal structure and Hirshfeld surface analysis of bis(caffeinium) hexachloridoplatinum(IV) in comparison with some related compounds (англ.) // Acta Crystallographica Section E: Crystallographic Communications. — 2023-06-01. — Vol. 79, iss. 7. — P. 644–647. — ISSN 2056-9890. — doi:10.1107/S2056989023005157. Архивировано 3 ноября 2023 года.
- ↑ Афанасьев А. В., Белова Е.В., Герман К.Э., Новиков А.П. Номенклатура,электронное строение органических соединений и новые подходык оценке их реакционной способности - Учебное пособие. — M.: [[Издательский дом "Граница" (издательство)|]], 2022. — 110 с. — ISBN 978-5-9933-0408-3.
Литература править
- Химическая Энциклопедия. Советская Энциклопедия. — М., 1988.
- В. В. Москва. Водородная связь в органической химии. Соросовский образовательный журнал, 11999,N 2, с.58-64 [3] Архивная копия от 7 сентября 2011 на Wayback Machine
- Пиментел Дж., О. Мак-Клеллан. Водородная связь, пер. с англ.. — М., 1964.
- Эпштейн Л.М, Шубина Е.С. Многоликая водородная связь // «Природа». — 2003. — № 1.
- Водородная связь. Сб. ст.. — М., 1964.
- Pauling L. The chemical bond. — N. Y., 1967.
Ссылки править
- Водородная связь — статья из энциклопедии «Кругосвет»
- Водородная связь / Иогансен А. В. // Большая советская энциклопедия : [в 30 т.] / гл. ред. А. М. Прохоров. — 3-е изд. — М. : Советская энциклопедия, 1969—1978.