Ингибиторы белка NS5A относятся к классу противовирусных препаратов прямого действия. Они направлены на белок NS5A вируса гепатита C. Их развитие является кульминацией более глубокого понимания жизненного цикла вируса[1][2]. Однако, их механизм действия сложен и не полностью изучен.
Ингибиторы белка NS5A должны быть использованы совместно с дополнительными противовирусными препаратами, так как они быстро приводят к развитию мутаций устойчивых к препарату[3].
Механизм действия
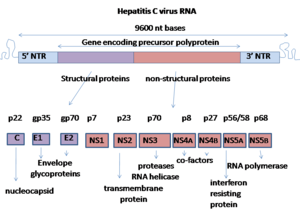
правитьВирус гепатита C — одноцепочечный РНК-вирус. Его репликация была исследована в гепатоцитах человека и шимпанзе. Транслируется один сложный белок вируса, который затем расщепляется клеточными и вирусными протеазами на три структурных белка[англ.] и семь неструктурных белков[англ.] (p7, NS2, NS3, NS4A, NS4B, NS5A, и NS5B)[4][5].
Ингибиторы белка NS5A приводят к значительному снижению РНК вируса гепатита C в крови и рассматриваются как мощный антивирусный препарат. Механизм их действия не полностью понят[6].
Большинство исследований сходятся в том, что эти ингибиторы действуют на двух основных этапах жизненного цикла вируса гепатита C: репликации геномной РНК и сборки вириона. Другие исследования предлагают фактор изменения клеток-хозяев, как возможный третий механизм[7].
По-видимому, ингибиторы белка NS5A препятствуют образованию новых комплексов репликации в результате постепенного замедления синтеза вирусной РНК. Влияние на ранее сформированные комплексы еще не выяснено[8].
Имеющиеся данные свидетельствуют о том, что ингибиторы белка NS5A изменяют расположение белка NS5A внутри клетки. Это может привести к нарушению сборки вирусов. Некоторые исследования показали, что ингибирование вирусной сборки играет ключевую роль в сокращении вирусной репликации РНК[9].
Исследования показали, что ингибиторы белка NS5A блокируют формирование перепончатой сети, которая защищает вирусный геном и особенности основных сайтов для вирусной репликации и сборки[10]. Этот механизм считается независимым от репликации РНК, но в нём могут быть задействованы ингибиторы белка NS5A, блокирующие формирование PI4KIIIα-NS5A-комплекса, необходимого для синтеза PI4P, что приводит к снижению целостности перепончатой сети, и, следовательно, уменьшению репликации РНК вируса гепатита C[11].
История
правитьРазработка противовирусных препаратов, способных мешать белкам, ответственным за репликацию вируса, тесно связана с достижениями в области технологий для создания эффективной культуры клеток, необходимых для экспериментов.
В 1999 году произошел прорыв в исследовании[12].
Первый ингибитор белка NS5A, который получил одобрение FDA в 2015 году, был даклатасвир[13]. Другие препараты были одобрены, среди них, в частности, ледипасвир, который, наряду с софосбувиром, входят в состав препарата Harvoni[14][15].
Ингибиторы белка NS5A были в центре внимания, когда они появились как часть первого лечения для вируса гепатита C в 2014 году[16]. Несмотря на недавнее появление многочисленных новых противовирусных препаратов, формирование резистентности по-прежнему вызывает озабоченность и поэтому эти ингибиторы всегда используется в сочетании с другими препаратами[17][18].
Структура
правитьАктивность ингибиторов чувствительна к изменениям в аминовой группе. Эти наблюдения показывают, что аминовая группа молекулы играет важную роль в ингибиторной активности[19].
| X | IC50 (nM) | Активность |
|---|---|---|
| >44 | Нет | |
| >44 | Нет | |
| 11 | Очень слабая | |
| 1.7 | Слабая | |
| 0.50 | Умеренная | |
| 3.7 | Слабая | |
| 0.11 | Умеренная | |
| 0.20 | Умеренная | |
| X | IC50 (nM) | Активность |
|---|---|---|
| >44 | Нет | |
| 0.071 | Умеренная | |
| 2.5 | Слабая | |
| 0.38 | Умеренная | |
| 0.20 | Умеренная | |
| 0.17 | Умеренная | |
| 0.040 | Сильная | |
| X | IC50 (nM) | Активность |
|---|---|---|
| CH2 | 0.094 | Сильная |
| CO | 0.30 | Умеренная |
| C(CH3)2 | 1.2 | Слабая |
Ссылки
править- ↑ Gogela N. A., Lin M. V., Wisocky J. L., Chung R. T. Enhancing our understanding of current therapies for hepatitis C virus (HCV). (англ.) // Current HIV/AIDS reports. — 2015. — Vol. 12, no. 1. — P. 68—78. — doi:10.1007/s11904-014-0243-7. — PMID 25761432.
- ↑ Pawlotsky, Jean-Michel. NS5A inhibitors in the treatment of hepatitis C (неопр.) // Journal of Hepatology. — 2013. — August (т. 59, № 2). — С. 375—382. — doi:10.1016/j.jhep.2013.03.030.
- ↑ Nakamoto, Shingo. Hepatitis C virus NS5A inhibitors and drug resistance mutations (англ.) // World Journal of Gastroenterology[англ.] : journal. — 2014. — Vol. 20, no. 11. — P. 2902. — doi:10.3748/wjg.v20.i11.2902. — PMID 24659881.
- ↑ Halliday, John. Vaccination for hepatitis C virus: closing in on an evasive target (англ.) // Expert Review of Vaccines[англ.] : journal. — 2014. — 9 January (vol. 10, no. 5). — P. 659—672. — doi:10.1586/erv.11.55. — PMID 21604986.
- ↑ Grakoui, A. Expression and identification of hepatitis C virus polyprotein cleavage products. (англ.) // Journal of Virology[англ.] : journal. — 1993. — 1 March (vol. 67, no. 3). — P. 1385—1395. — ISSN 0022-538X. — PMID 7679746.
- ↑ Ahmed, Marawan. A Comprehensive Computational Analysis for the Binding Modes of Hepatitis C Virus NS5A Inhibitors: The Question of Symmetry (англ.) // ACS Infectious Diseases : journal. — 2016. — 3 August (vol. 2). — P. 872—881. — doi:10.1021/acsinfecdis.6b00113.
- ↑ Issur, Moheshwarnath. Resistance Patterns Associated with HCV NS5A Inhibitors Provide Limited Insight into Drug Binding (англ.) // Viruses : journal. — 2014. — 6 November (vol. 6, no. 11). — P. 4227—4241. — doi:10.3390/v6114227.
- ↑ Guedj, J. Modeling shows that the NS5A inhibitor daclatasvir has two modes of action and yields a shorter estimate of the hepatitis C virus half-life (англ.) // Proceedings of the National Academy of Sciences of the United States of America : journal. — 2013. — 19 February (vol. 110, no. 10). — P. 3991—3996. — doi:10.1073/pnas.1203110110. — PMID 23431163.
- ↑ McGivern, David R. Kinetic Analyses Reveal Potent and Early Blockade of Hepatitis C Virus Assembly by NS5A Inhibitors (англ.) // Gastroenterology : journal. — 2014. — August (vol. 147, no. 2). — P. 453—462.e7. — doi:10.1053/j.gastro.2014.04.021. — PMID 24768676.
- ↑ Neufeldt, Christopher J. The Hepatitis C Virus-Induced Membranous Web and Associated Nuclear Transport Machinery Limit Access of Pattern Recognition Receptors to Viral Replication Sites (англ.) // PLOS Pathogens : journal. — 2016. — 10 February (vol. 12, no. 2). — P. e1005428. — doi:10.1371/journal.ppat.1005428.
- ↑ Berger, Carola. Daclatasvir-Like Inhibitors of NS5A Block Early Biogenesis of Hepatitis C Virus–Induced Membranous Replication Factories, Independent of RNA Replication (англ.) // Gastroenterology : journal. — 2014. — November (vol. 147, no. 5). — P. 1094—1105.e25. — doi:10.1053/j.gastro.2014.07.019. — PMID 25046163.
- ↑ Lohmann, V. Replication of Subgenomic Hepatitis C Virus RNAs in a Hepatoma Cell Line (англ.) // Science : journal. — 1999. — 2 July (vol. 285, no. 5424). — P. 110—113. — doi:10.1126/science.285.5424.110.
- ↑ "FDA approves new treatment for chronic hepatitis C genotype 3 infections". FDA. 2015-07-27. Архивировано 3 октября 2016. Дата обращения: 29 сентября 2016.
- ↑ Link, John O. Discovery of Ledipasvir (GS-5885): A Potent, Once-Daily Oral NS5A Inhibitor for the Treatment of Hepatitis C Virus Infection (англ.) // Journal of Medicinal Chemistry[англ.] : journal. — 2014. — 13 March (vol. 57, no. 5). — P. 2033—2046. — doi:10.1021/jm401499g.
- ↑ Keating, Gillian M. Ledipasvir/Sofosbuvir: A Review of Its Use in Chronic Hepatitis C (англ.) // Drugs[англ.] : journal. — Adis International, 2015. — 3 April (vol. 75, no. 6). — P. 675—685. — doi:10.1007/s40265-015-0381-2. — PMID 25837989.
- ↑ Do A., Mittal Y., Liapakis A., Cohen E., Chau H., Bertuccio C., Sapir D., Wright J., Eggers C., Drozd K., Ciarleglio M., Deng Y., Lim J. K. Drug Authorization for Sofosbuvir/Ledipasvir (Harvoni) for Chronic HCV Infection in a Real-World Cohort: A New Barrier in the HCV Care Cascade. (англ.) // Public Library of Science ONE. — 2015. — Vol. 10, no. 8. — P. e0135645. — doi:10.1371/journal.pone.0135645. — PMID 26312999.
- ↑ Fridell R. A., Qiu D., Wang C., Valera L., Gao M. Resistance analysis of the hepatitis C virus NS5A inhibitor BMS-790052 in an in vitro replicon system. (англ.) // Antimicrobial agents and chemotherapy. — 2010. — Vol. 54, no. 9. — P. 3641—3650. — doi:10.1128/AAC.00556-10. — PMID 20585111.
- ↑ Asselah T., Boyer N., Saadoun D., Martinot-Peignoux M., Marcellin P. Direct-acting antivirals for the treatment of hepatitis C virus infection: optimizing current IFN-free treatment and future perspectives. (англ.) // Liver international : official journal of the International Association for the Study of the Liver. — 2016. — Vol. 36 Suppl 1. — P. 47—57. — doi:10.1111/liv.13027. — PMID 26725897.
- ↑ Romine, Jeffrey L. Inhibitors of HCV NS5A: From Iminothiazolidinones to Symmetrical Stilbenes (англ.) // ACS Medicinal Chemistry Letters[англ.] : journal. — 2011. — 10 March (vol. 2, no. 3). — P. 224—229. — doi:10.1021/ml1002647.