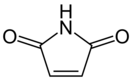
Малеимид
Малеимид – химическое соединение с формулой H2C2(CO)2NH. Ненасыщенный циклический имид, имеющий важное значение в органическом синтезе и биоконжугировании (модифицировании биологогических объектов). Название образовывается при слиянии полного химического названия соединения: "малеиновой кислоты имид". Малеимидами также называют класс органических соединий, образующихся из незамещенной молекулы малеимида посредством замещения атома водорода (N-H) на алкильный или арильный радикал (N-R). В роли заместителя R может также выступать молекулярное соединение (к примеру, биотин), флуоресцентный краситель, олигосахарид, нуклеиновая кислота, реакционная химическая группа (для проведения последующей химической реакции), синтетический полимер (к примеру, полиэтиленгликоль), или молекула белка.[2]
| Малеимид | |||
|---|---|---|---|
| |||
| Общие | |||
| Систематическое наименование |
1H-пиррон-2,5-дион | ||
| Хим. формула | C4H3NO2 | ||
| Термические свойства | |||
| Температура | |||
| • плавления | 92 °C[1] | ||
| Классификация | |||
| Рег. номер CAS | 541-59-3 | ||
| PubChem | 10935 | ||
| Рег. номер EINECS | 208-787-4 | ||
| SMILES | |||
| InChI | |||
| ChEBI | 16072 | ||
| ChemSpider | 10471 | ||
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |||
Органическая химия
правитьМалеимиды и их производные образуются при реакции малеинового ангидрида с аминами с последующей дегидратацией образующегося на первом этапе нециклического амида.[3] Наиболее важным химическим свойством малеимидов является их исключительная реакционная способность в реакции cопряжённого присоединения по Михаэлю и реакции Дильса-Альдера.' Бисмалеимидами' называют класс соединений, содержащий два малеимидовых остатка, ковалентно соединённых между собой. В случае, если остаток малемида соединён с другой реактивной группой (например, активированным эфиром кислоты), полученные соединения называются гетеробифункциональными реагентами на основе малеимида и находят частое применение при модифицировании протеинов и других биологических объектов (биоконъюгирование).[2]
Природные малеимиды
правитьИз-за своей высокой реакционной способности, очень небольшое количество природных соединений содержит малеимидовый остаток. Примером таких соединений являются цитотоксичный шоудомицин, выделенный из Streptomyces showdoensis,[4] и пенколид, выделенный из Pe. multicolor.[4]
Применение в биотехнологии
правитьМетодологии основанные на применении малеимида являются одними из наиболее популярных в биоконъюгировании (модифицированнии биологических объектов).[5][6] Из-за высокой скорости и селективности реакции производных малеимида с тиольнымиостатками цистеина в протеинах, большое количество гетеробифункциональных производным малеимида используется в современной биотехнологии для получения таргетных лекарственных средств, изучения, конъюгирования и иммобилизации всевозможных белков (к примеру, ферментов или антител).[7] Кроме того реакции малеимид-тиол могут использоваться при ПЭГилировании тиол-содержащих поверхностей наночастиц.[8]
Благодаря возможности протекания реакции тиол-малеимид при физиологических условиях, полимерные материалы и липосомы, модифицированные функциональными группами малеимида, показали высокую способность к адгезии к слизистым тканям.[9][10]
Примечания
править- ↑ Bradley J., Williams A., Andrew S.I.D. Lang Jean-Claude Bradley Open Melting Point Dataset // (unknown type) — 2014. — doi:10.6084/M9.FIGSHARE.1031637.V2
- ↑ 1 2 Hermanson, Greg. Bioconjugate Techniques (неопр.). — Elsevier. — С. 299—339. — ISBN 978-0-12-382239-0. Архивировано 6 апреля 2018 года.
- ↑ Cava, M. P.; Deana, A. A.; Muth, K.; Mitchell, M. J. (1973), "N-Phenylmaleimide", Org. Synth.[англ.]
{{citation}}: Википедия:Обслуживание CS1 (множественные имена: authors list) (ссылка); Coll. Vol., 5: 944{{citation}}:|title=пропущен или пуст (справка) - ↑ 1 2 J. H. Birkinshaw, M. G. Kalyanpur and C. E. Stickings. Studies on the biochemistry of microorganisms. 113. Pencolide, a nitrogen-containing metabolite of Penicillium multicolor Grigorievna-Manilova and poradievova (англ.) // Biochem. J.[англ.] : journal. — 1963. — Vol. 86. — P. 237—243.
- ↑ Koniev, O.; Wagner, A. Developments and recent advancements in the field of endogenous amino acid selective bond forming reactions for bioconjugation (англ.) // Chem. Soc. Rev.[англ.] : journal. — 2015. — Vol. 44, no. 15. — P. 5495—5551. — doi:10.1039/C5CS00048C.
- ↑ Francis, M. B.; Carrico, I. S. New frontiers in protein bioconjugation (англ.) // Current Opinion in Chemical Biology. — Elsevier, 2010. — Vol. 14, no. 6. — P. 771—773. — doi:10.1016/j.cbpa.2010.11.006. — PMID 21112236.
- ↑ Hermanson, Greg. Bioconjugate Techniques (неопр.). — Elsevier. — С. 1—125. — ISBN 978-0-12-382239-0. Архивировано 6 апреля 2018 года.
- ↑ Galiya S. Irmukhametova, Grigoriy A. Mun, Vitaliy V. Khutoryanskiy. Thiolated Mucoadhesive and PEGylated Nonmucoadhesive Organosilica Nanoparticles from 3-Mercaptopropyltrimethoxysilane // Langmuir. — 2011-08-02. — Т. 27, вып. 15. — С. 9551—9556. — ISSN 0743-7463. — doi:10.1021/la201385h.
- ↑ Vitaliy V. Khutoryanskiy, Praneet Opanasopit, Ruairí P. Brannigan, Prasopchai Tonglairoum. Maleimide-bearing nanogels as novel mucoadhesive materials for drug delivery (англ.) // Journal of Materials Chemistry B. — 2016-10-12. — Vol. 4, iss. 40. — P. 6581—6587. — ISSN 2050-7518. — doi:10.1039/C6TB02124G. Архивировано 11 августа 2019 года.
- ↑ Daulet B. Kaldybekov, Prasopchai Tonglairoum, Praneet Opanasopit, Vitaliy V. Khutoryanskiy. Mucoadhesive maleimide-functionalised liposomes for drug delivery to urinary bladder // European Journal of Pharmaceutical Sciences. — 2018-01-01. — Т. 111. — С. 83—90. — ISSN 0928-0987. — doi:10.1016/j.ejps.2017.09.039. Архивировано 11 августа 2019 года.
Ссылки
правитьНа эту статью не ссылаются другие статьи Википедии. |